一、產業規范政策
醫療器械行業的主管部門主要為國家發展和改革委員會、國家藥品監督管理局和國家衛生健康委員會,而我國體外診斷行業在行政管理上歸屬于醫療器械管理,因此該行業的產品規范較為嚴格。
產業規范政策
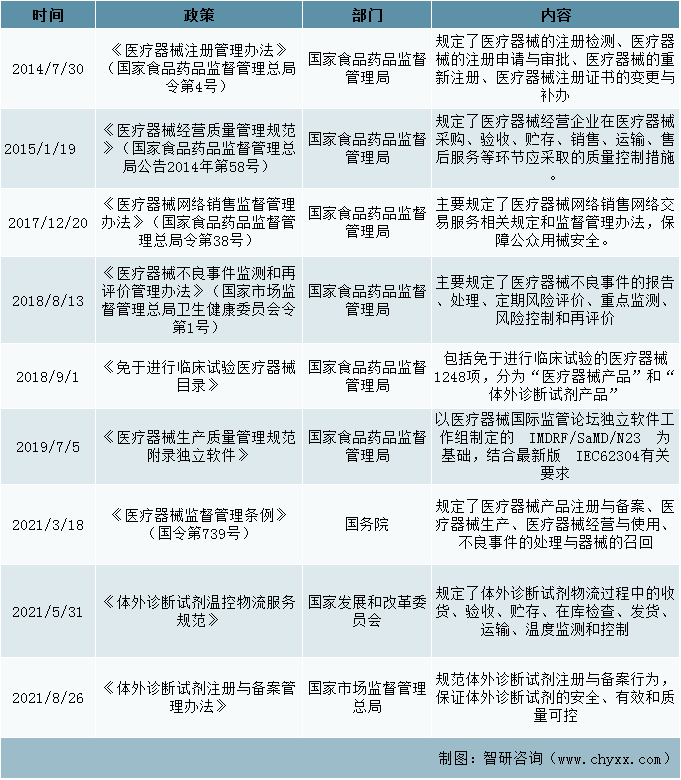
資料來源:智研咨詢整理
二、發展規劃政策
體外診斷在整個醫療服務過程中占據著舉足輕重的地位,它可以幫助醫生快速準確地發現病人體內存在的病變,從而及時做出正確的診斷并采取相應措施。在《“十四五”國家藥品安全及促進高質量發展規劃》中,明確規劃了在體外診斷試劑等領域開展醫療器械監管科學重點實驗室建設,健全應急審評審批、檢驗檢測、監督檢查機制,完善藥品儲備和供應制度。
發展規劃政策
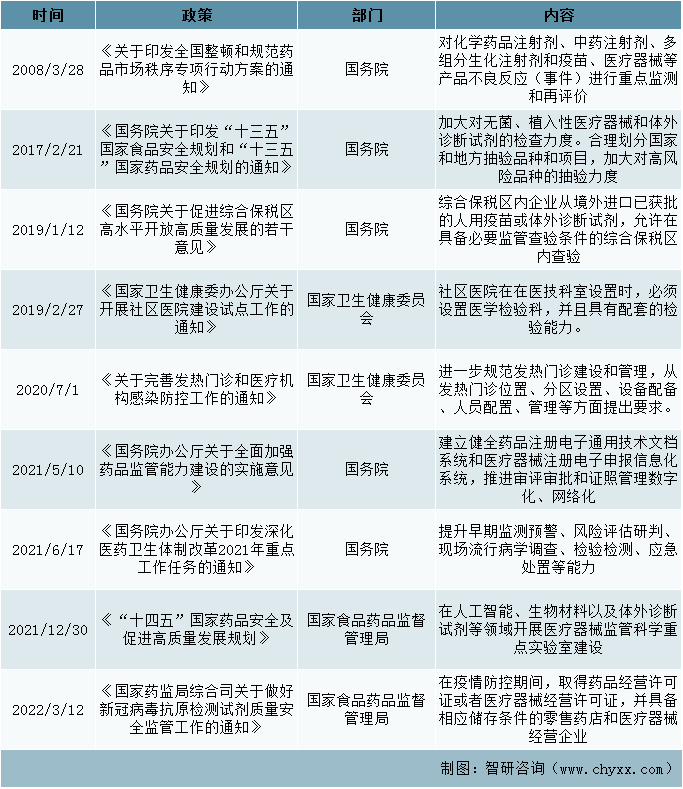
資料來源:智研咨詢整理
三、監督管理政策
針對體外診斷發展背景及發展條件,對其出臺一系列監管政策。其中在《國家藥監局綜合司關于開展醫療器械質量安全風險隱患排查治理工作的通知》中,按照2021年全國醫療器械監督管理工作會議部署,為深入貫徹落實“四個最嚴”要求,強化醫療器械風險管理。而在2020年的《國家醫療器械不良事件監測年度報告》中,全面反映2020年我國醫療器械不良事件監測工作情況,國家藥品不良反應監測中心收到的醫療器械不良事件報告中,涉及體外診斷試劑的報告3,672份,占報告總數的0.69%。
監督管理政策
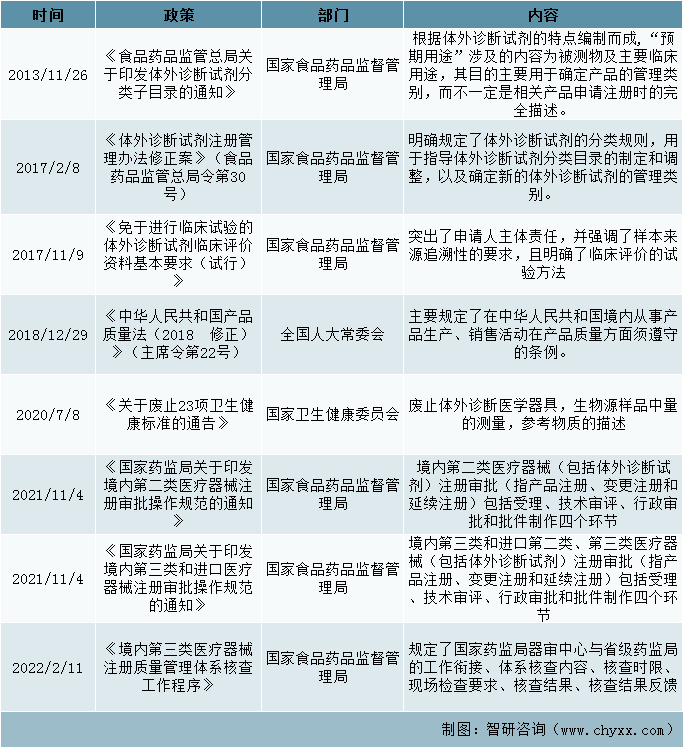
資料來源:智研咨詢整理
四、鼓勵支持政策
在獎勵補貼方面,體外診斷行業作為重點鼓勵發展的行業,國家產業政策對行業的發展具有積極的促進作用,近年來我國陸續出臺一系列法律法規和產業政策,扶持體外診斷產業發展。
鼓勵支持政策(一)
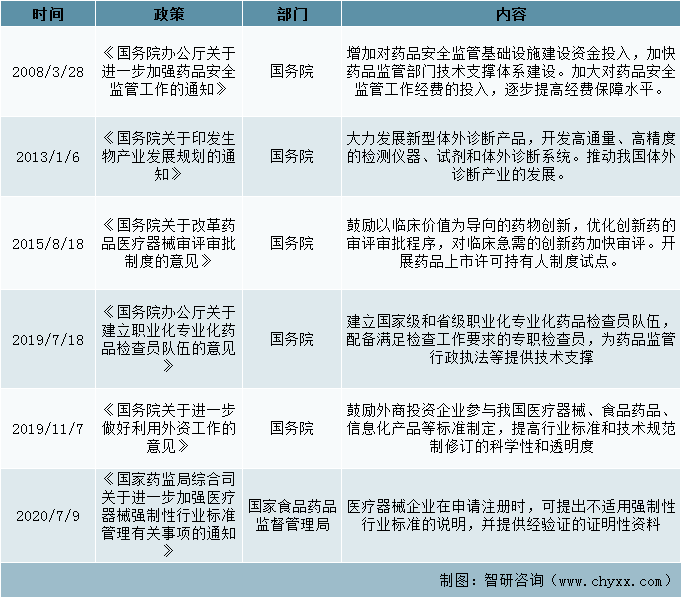
資料來源:智研咨詢整理
在財政局頒發布的《市財政助力研究型病房建設工作穩步推進》中,疫情期間地壇醫院啟動了藥物和體外診斷試劑的臨床試驗共12項,將倫理審查的快審周期由原來的5天縮短至3天,有效地支持了萬泰生物、卓誠惠生、熱景生物等多家北京企業試劑盒的研發。且在《國家藥監局綜合司關于開展2021年全國醫療器械安全宣傳周活動的通知》中,加強醫療器械創新技術的宣傳,鼓勵醫療器械新技術應用,促進科學成果的轉化與應用。貫徹新發展理念,聚焦新時代監管改革創新,為企業研發創新提供更多的優質服務。
鼓勵支持政策(二)
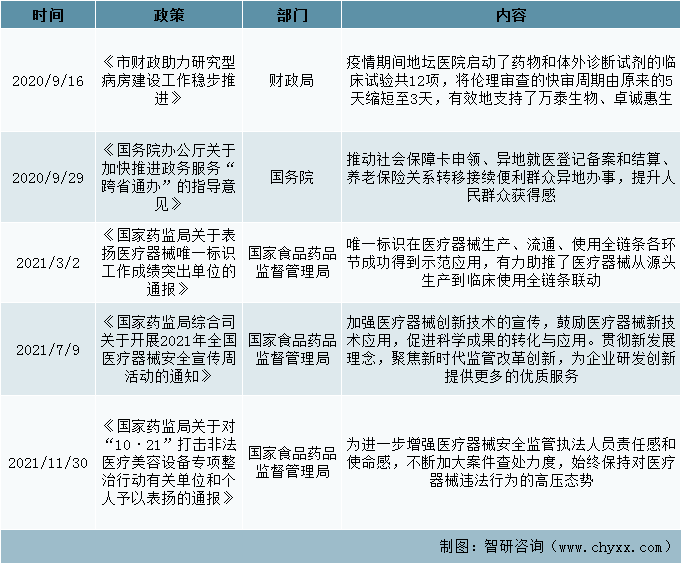
資料來源:智研咨詢整理
五、科技技術政策
技術政策在2010年10月18日的《國務院關于加快培育和發展戰略性新興產業的決定》中提出生物產業作為七大戰略性新興產業之一,要成為國民經濟的支柱產業之一,并指出要大力發展重大疾病防治的生物技術藥物、新型疫苗和診斷試劑、化學藥物、現代中藥等創新藥物大品種,提升生物醫藥產業水平。其中實施生物疫苗和診斷試劑高技術產業化專項,其中診斷試劑以免疫診斷、分子診斷等新型檢測試劑為重點。其中在開展重大疾病體外診斷試劑及性能評價量值溯源技術研究,研制診斷試劑溯源用高端標準物質,研究臨床診斷及病理學成像溯源技術,解決診斷試劑測量準確性和一致性問題,提升國產試劑產品質量與市場競爭力。
科技技術政策
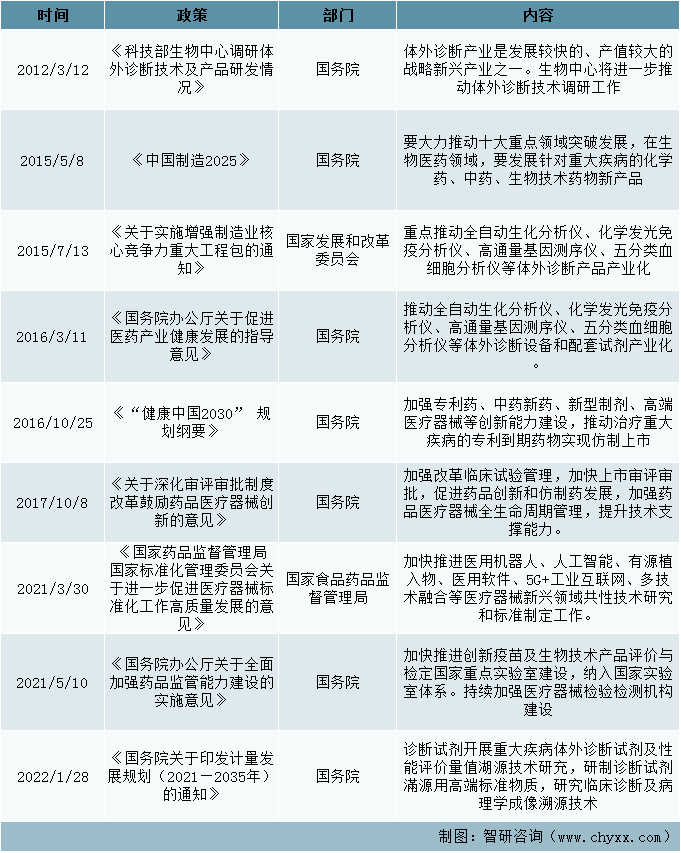
資料來源:智研咨詢整理
以上數據及信息可參考智研咨詢(www.szxuejia.com)發布的《2022-2028年中國體外診斷行業市場發展現狀及競爭格局預測報告》。智研咨詢是中國領先產業咨詢機構,提供深度產業研究報告、商業計劃書、可行性研究報告及定制服務等一站式產業咨詢服務。您可以關注【智研咨詢】公眾號,每天及時掌握更多行業動態。
 智研咨詢 - 精品報告
智研咨詢 - 精品報告

2025-2031年中國體外診斷行業市場發展現狀及競爭格局預測報告
《2025-2031年中國體外診斷行業市場發展現狀及競爭格局預測報告》共十六章,包含2025-2031年體外診斷行業面臨的困境及對策,體外診斷行業發展戰略研究,研究結論及發展建議等內容。

 公眾號
公眾號
 小程序
小程序
 微信咨詢
微信咨詢




















![2021年中國體外診斷行業主要企業經營現狀分析,產品持續突破,市場前景廣闊[圖]](http://img.chyxx.com/images/2022/0408/1ba88a0bac4b4a65439b806124f6fc0f4ab03cad.png?x-oss-process=style/w320)

![2022年中國體外診斷行業發展環境(PEST)分析:社會疾病預防需求持續刺激行業發展[圖]](http://img.chyxx.com/images/2022/0330/83e55e0fd01cd7eb3b56b758f35281ec8d2514ab.png?x-oss-process=style/w320)
![中國體外診斷行業產業鏈全景分析及產業發展痛點分析[圖]](http://img.chyxx.com/images/2022/0330/dd2a6e2dd1963d26c8672c625ba6166e69bd4120.png?x-oss-process=style/w320)